
编者按
类器官(Organoid)作为新型实验模型,较好地保留了其起源组织的形态表型、细胞功能、生物学行为以及基因谱特征。因其可体外培养、低温保藏和复苏再利用又有“活组织库”(living biobank)之称。类器官作为实验动物的替代品在新药研发及药物敏感性筛选中担当重要角色,其质量好坏直接影响到实验精准性,故规范与制定类器官构建各环节的标准迫在眉睫。类器官构建领域存在两大主流方向:成体干细胞(ASC)源性类器官(又称患者源性类器,PDO)和诱导性多潜能干细胞(iPSC)/胚胎干细胞(ESC)源性类器官。
今天,我们分享一项由瑞金医院普外科/上海消化外科研究所于颖彦教授、生物芯片上海国家工程研究中心郜恒骏教授团队于2024年11月联合发表在《Chinese Medical Journal》(IF=7.5,Q1)的成果,通过聚焦于成体干细胞源性类器官,系统地阐述类器官构建的规范性操作流程、类器官培养相关实验室标准化建设、国内外已经出台的类器官相关标准或指南性文件,并提出该领域存在的挑战和未来发展方向。
文章题目
Living biobank: standardization of organoid construction and challenges
杂志:Chinese Medical Journal(IF=7.5,Q1)
发表时间:2024年12月5日
作者:杨蕊馨博士、郜恒骏教授、于颖彦教授等
单位:瑞金医院普外科、上海消化外科研究所、生物芯片上海国家工程研究中心
01、研究背景
在生物医药领域,药物研发、疾病诊断与治疗以及致病机制的研究均离不开实验模型。比如细胞系与实验动物。前者在体外长期培养中历经基因组变异压力的选择,已难以反映原始肿瘤的生物学行为和对药物治疗反应。故利用肿瘤细胞系开展的药物筛选体外治疗有效,但在后续临床试验中失败的案例屡见不鲜。而实验中常用的动物模型,比如免疫缺陷小鼠动物模型和人源性异种移植瘤模型,在疾病与肿瘤的发病机制研究、新型分子靶点鉴定以及临床前治疗药物敏感性评价中可发挥一定作用,但因缺乏完整的免疫系统,与人类生长体系尚存在相当的差异。
2009年问世的类器官作为新型实验模型,可以实现对多种组织细胞的体外培养、低温保藏和复苏后再利用,作为体外活组织库受到生物医药界青睐。2022年底,美国FDA通过的一项新法案提出,新药的临床前研究可不再强制进行动物实验,可采用类器官芯片或人工智能等新技术作为替代品,奠定了类器官这种新型实验模型在新药研发中的地位。随着类器官在生物医药研究、临床转化研究应用范围扩大,该领域中的技术标准制定与实施问题应运而生。
类器官构建的标准化是指对组织样本前处理、3D细胞培养、类器官传代、类器官冻存、类器官复苏、类器官表型鉴定、类器官基因谱分析以及类器官质量评估等多环节进行规范化操作和管理,确保产出的类器官质量高且性能稳定。
我国标准化体系分成五个层级:国家标准、行业标准、地方标准、团体标准和企业标准。自2022年初首个《人胃肠上皮组织类器官的构建与保藏操作指南》团体标准(T/CMBA 017-2022)发布并实施以来,截止到2024年6月,国内外已经有多部类器官相关的团体标准及临床诊治指南问世,为不同组织细胞源性类器官构建及临床应用提供了指导性文件。
类器官模型研发及标准化建设仍处于早期发展阶段,多种组织细胞来源的标准及疾病模型尚处于空白。已经出台的类器官相关标准主要为团体标准,尚未上升到国家标准层面。国际上也缺乏类器官构建统一的标准。此外,更加仿真的类器官构建技术还在研发阶段,比如实体肿瘤类器官与肿瘤微环境细胞的共培养体系需要不断完善,组织细胞类器官与病原微生物的共培养系统需要探索。
除了本文介绍的成体干细胞源性类器官外,iPSC/ESC源的类器官构建也需要进一步加强,从而解决某些罕见单基因遗传性疾病等缺乏研究模型的问题。随着人工智能自动化技术的发展,标准化类器官培养技术与人工智能相结合,可以促进类器官培养的自动化,提高质量评估的精准性与效率。标准化类器官培养技术与临床大数据或基因组大数据相结合,有助于新药研发及药物敏感性精准预测。
02、研究成果
1. 类器官构建标准化
类器官构建的标准化,涵盖组织样本前处理、3D细胞培养、类器官传代、冻存、复苏、表型鉴定、基因谱分析以及质量评估等多个环节,旨在确保产出的类器官具备高质量和稳定性能,对推动类器官技术从实验室研究走向临床应用与产业化发展,具有重要的意义(图1)。

图1 类器官构建的关键步骤
1.1 组织收集与预处理
在组织收集和预处理阶段,需严格遵循人类生物库伦理要求。专业医生需在30分钟内对新鲜人体组织样本进行处理,样本大小不小于5×5mm,放入含抗生素的DMEM/F12保存液。若不能当日培养,需使用含Y27632的保存液过夜,并在24小时内开始类器官培养。预处理过程包括彻底清洗组织,用含抗生素的PBS洗涤,切割后振荡洗涤、离心并丢弃浑浊液,重复洗涤三次。
1.2 类器官培养
类器官培养时,消化酶和时间需依据组织类型灵活调整。例如,胃肠道等组织需在37℃下用含胶原酶和透明质酸酶的消化液处理,胃肠道、食管和肺组织消化约1小时,肝脏30分钟,肾脏15分钟。消化后过滤、离心得到细胞球,加入DMEM/F12培养基与基质胶混合接种于孔板,37℃孵育后添加完全培养基培养,每3 - 5天换液,2周后可传代。
1.3 类器官传代
细胞培养两周后进行类器官传代,使用TrypLETM Express酶将类器官消化成单细胞,重悬于与Matrigel混合的高级DMEM/F12培养基中,按1:1比例接种于24孔板,传代比例通常为1:2或1:4 ,代数少于10为早期,10-20代为中期,超过20代为后期。
1.4 类器官低温贮藏与复苏
为建立体外活生物库,细胞传代时约2/3细胞用于冷冻保存。将细胞与CryoStor® CS10冷冻液混合,置于-80°C冷冻盒过夜,次日转移至液氮罐长期保存。类器官复苏基于快速解冻原理,将冷冻管放入37°C水浴中摇晃加速融化,融化后转移到离心管,加入DMEM/F12培养基离心,去除上清液保留沉淀,重悬于Matrigel混合培养基,按1:1比例接种于24孔板,37℃培养箱培养30分钟后加入完全培养基继续培养。
1.5 废弃类器官处理
若类器官培养中基质或培养基3天内变混浊,可能是真菌或细菌污染,需丢弃;怀疑支原体污染时,可尝试使用去除剂,无效则需丢弃,并按生物医学废物规定处理。
2. 类器官的分子特性及质量控制
类器官虽能保留亲本组织的遗传特征和生物学功能,但长期传代、冷冻保存、复苏和再培养对其分子特性的影响研究尚不充分。研究显示,短期传代类器官基因突变漂移率低,长期传代则会显著增加基因突变漂移率 。可利用基因组学方法如WGS、WES、RNA-seq和scRNA-seq进行分子分析,通过核型分析和STR检测鉴定类器官系。评估类器官质量的方法包括形态学观察、多种染色技术和ATP含量检测(图2)。

图2 类器官评价采用多种评价方法
3. 实验室标准化建设
构建高质量类器官离不开完善的实验室设施。在中国,根据实验目的不同,细胞培养室通常分为三层结构(图3)。
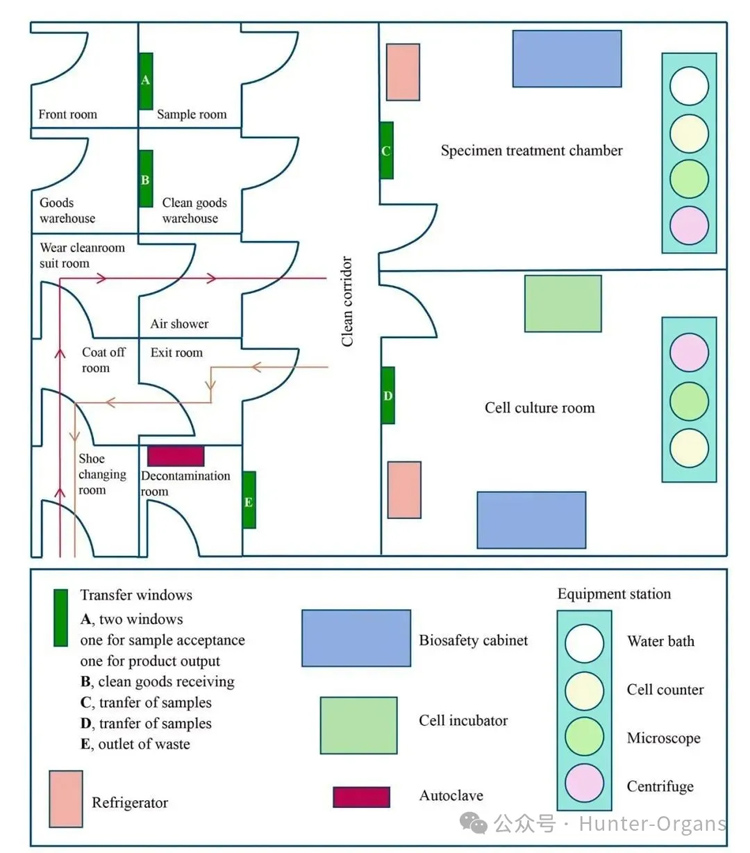
图3 标准化细胞培养室的布局
3.1 基础研究细胞培养室
需遵循《洁净室设计规范》,环境洁净等级至少满足D+A级。实验室内设备精简,设有物料和样品专用入口及特殊出口,研究人员通过换鞋、换衣和空气淋浴的三层缓冲区进入。室内有严格的洁净等级和细菌标准,温度、湿度需控制,通风量需达标,所有操作在净化工作台上进行,工作人员需提前开启空气净化系统和紫外线灯。
3.2 药物开发细胞培养室
专为新药筛选、药敏试验等设计,洁净等级至少达到C+A级。C级标准对静态和动态下粉尘颗粒数、浮游细菌和沉积物细菌标准,以及温度、湿度和通风频率都有明确规定。实验操作在A级生物安全柜上进行,工作人员进入流程与基础研究细胞培养室相同,且设有单独出口避免交叉污染。
3.3 生产治疗级生物药品细胞培养室
根据《医药行业洁净车间设计标准》,洁净标准至少达到B+A级。B级洁净区在静态和动态条件下对粉尘颗粒数限制严格,浮游细菌和沉积物细菌标准更严苛,环境温度和湿度也有具体要求。实验操作在A级生物安全柜中进行,工作人员进入流程一致,设有单独出口避免交叉污染,且细胞培养室需定期消毒(表1)。

表1
4. 国内外类器官相关标准现状
我国标准化体系包含国家标准、行业标准、地方标准、团体标准和企业标准五个层级。自2022年初首个《人胃肠上皮组织类器官的构建与保藏操作指南》团体标准发布实施以来,截至2024年6月,国内外已出台多部类器官相关团体标准及临床诊治指南,为不同组织细胞源性类器官构建及临床应用提供了指导。但类器官模型研发及标准化建设仍处于早期,多种组织细胞来源的标准及疾病模型尚属空白,已出台标准多为团体标准,未上升到国家标准层面,国际上也缺乏统一标准(图4)。
图4 类器官相关标准或指南的时间表
03、类器官构建面临的挑战与未来方向
目前,类器官模型研发及标准化建设仍处于早期发展阶段,多种组织细胞来源的标准及疾病模型尚处于空白。已经出台的类器官相关标准主要为团体标准,尚未上升到国家标准层面。国际上也缺乏类器官构建统一的标准。
此外,更加仿真的类器官构建技术还在研发阶段,比如实体肿瘤类器官与肿瘤微环境细胞的共培养体系需要不断完善,组织细胞类器官与病原微生物的共培养系统需要探索。
除了本文介绍的成体干细胞源性类器官外,iPSC/ESC源的类器官构建也需要进一步加强,从而解决某些罕见单基因遗传性疾病等缺乏研究模型问题。随着人工智能自动化技术的发展,标准化类器官培养技术与人工智能相结合,可以促进类器官培养的自动化,提高质量评估的精准性与效率。标准化类器官培养技术与临床大数据或基因组大数据相结合,有助于新药研发及药物敏感性精准预测。
作为健康美丽产业CRO服务开拓者与引领者、斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、类器官、哺乳动物、人体”多维生物技术服务体系,开展健康美丽CRO服务、科研服务、智慧实验室搭建三大业务。目前,环特已建立200多种斑马鱼模型,胃癌、脑类器官、心脏类器官及各种肿瘤类器官培养平台,欢迎有需要的读者垂询!
